Technologie unikalnej identyfikacji wyrobów automatyzują odczyt identyfikatorów medycznych i kodów kreskowych
Przekazane przez: Północnoamerykańscy redaktorzy DigiKey
2023-10-26
W 2013 r. Amerykańska Agencja ds. Żywności i Leków (FDA) wdrożyła system unikalnej identyfikacji wyrobów medycznych UDI (Unique Device Identification). Zasady te miały na celu poprawę bezpieczeństwa pacjentów poprzez zapewnienie spójnej metody śledzenia i identyfikacji wyrobów medycznych przy użyciu nowoczesnej dokumentacji w miejscach produkcji, dystrybucji i użytkowania. Podobnie jak wymagania przepisów dotyczących wyrobów medycznych w Europie lub podobne przepisy w innych krajach, amerykańskie przepisy dotyczące unikalnej identyfikacji wyrobów medycznych (UDI) zwiększają dokładność raportowania i ułatwiają analizę w przypadku wycofania lub zdarzenia niepożądanego.
Od 24 września 2023 r. FDA będzie w pełni egzekwować krajowe przepisy dotyczące przedmiotów związanych ze zdrowiem i numery kodów leków na etykietach i opakowaniach wyrobów. Wszelkie produkty medyczne oznakowane w tym dniu lub później muszą być w pełni zgodne z wymogami UDI. Wspomniane przepisy będą miały wpływ na następujące kwestie:
- Produkty klasy 3 o krytycznym znaczeniu dla życia, takie jak rozruszniki serca i wszczepiane protezy
- Produkty klasy 2 o umiarkowanym ryzyku, takie jak strzykawki, cewniki i szwy wchłanialne
- Produkty niższego ryzyka klasy 1, takie jak nici dentystyczne, fartuchy medyczne i maski tlenowe
Pełne egzekwowanie tych przepisów oznacza, że jeżeli wyrób medyczny nie posiada kodu kreskowego umożliwiającego zeskanowanie, nie będzie już uważany za produkt prawidłowy i nadający się do użytku, nawet jeśli znajdują się na nim etykiety czytelne dla człowieka i nawet jeśli ogólnie przyjmuje się, że produkt jest łatwo rozpoznawalny przez większość użytkowników. Pełne egzekwowanie przepisów spowoduje wszechstronne przyjęcie przez branżę medyczną i rozliczanie ubezpieczeń medycznych.
 Ilustracja 1: niektóre ręczne weryfikatory kodów kreskowych DPM (Direct Part Mark) są wyposażone w zaawansowane oświetlenie i oprogramowanie do automatycznego wyszukiwania symboli i przełączania ustawień w celu optymalizacji odczytu konkretnego znaku DPM i podłoża materiałowego. W rzeczywistości przedstawiony tutaj aparat LVS-9585 może weryfikować zarówno części oznaczone metodą DPM, jak i drukowane etykiety w celu kompleksowej analizy i raportowania. (Źródło ilustracji: Omron Automation)
Ilustracja 1: niektóre ręczne weryfikatory kodów kreskowych DPM (Direct Part Mark) są wyposażone w zaawansowane oświetlenie i oprogramowanie do automatycznego wyszukiwania symboli i przełączania ustawień w celu optymalizacji odczytu konkretnego znaku DPM i podłoża materiałowego. W rzeczywistości przedstawiony tutaj aparat LVS-9585 może weryfikować zarówno części oznaczone metodą DPM, jak i drukowane etykiety w celu kompleksowej analizy i raportowania. (Źródło ilustracji: Omron Automation)
Odpowiedzialność spoczywa na podmiocie zamawiającym (właścicielu marki)
W Stanach Zjednoczonych posiadacz własności intelektualnej i marka każdego produktu medycznego skierowanego do użytkowników jest odpowiedzialna za dokładność i jakość kodów UDI. Jest to szczególnie ważne w sytuacji, w której znaczna część produktów medycznych na rynku jest wytwarzana na zlecenie i zlecana do zakładów innych organizacji. W związku z tym, obowiązkiem organizacji zamawiającej jest zapewnienie, że cały łańcuch dostaw jest zgodny z wymogami UDI i produkuje dokładne etykiety.
Pochodzenie technologii unikalnej identyfikacji wyrobów medycznych
UDI to statyczne identyfikatory wyrobów medycznych. Jednakże zmiana liczby sztuk w opakowaniu może spowodować konieczność wprowadzenia nowego identyfikatora. Agencje wydające zezwolenia dyktują, w jaki sposób te szczegóły są rozróżniane. Również zmiana warunków sterylności opakowania wyrobu może spowodować zmianę jego identyfikatora. Zmiana rynku docelowego wyrobu (kraju, w którym wyrób będzie sprzedawany), języka etykiety lub znaku CE może również wymagać zmiany identyfikatora wyrobu.
Przed wprowadzeniem przepisów dotyczących unikalnej identyfikacji wyrobów medycznych (UDI), producent wyrobów medycznych mógł oznaczać produkt określonym numerem katalogowym. Ten numer katalogowy mógł zostać zmieniony przez dystrybutora, a następnie przez podmiot świadczący opiekę zdrowotną lub szpital. Ze względu na możliwość zmiany numeru katalogowego przez każdy podmiot przed dotarciem do pacjenta, prawie niemożliwe było skuteczne śledzenie produktów, obsługiwanie wycofywania produktów z rynku, zapobieganie fałszerstwom lub dokładne zamawianie nowych zapasów.
Powiązane tematy: wdrażanie niezawodnych rozwiązań w zakresie identyfikowalności
Obecnie każdemu wyrobowi nadawany jest ustandaryzowany i stały identyfikator zwany UDI, aby umożliwić wszystkim podmiotom szybszą i precyzyjną identyfikację wyrobu, ostatecznie ograniczając liczbę błędów medycznych. Identyfikator UDI jest kodem alfanumerycznym zawierającym dwa kluczowe elementy danych:
- Identyfikator wyrobu
- Identyfikator produkcyjny
Identyfikator wyrobu to statyczna etykieta przypisana do danego wyrobu, zawierająca informację o podmiocie nakładającym etykietę (zwykle producencie urządzenia) i konkretny numer modelu wyrobu. Natomiast identyfikator produkcyjny zawiera dane, które mogą się różnić, a większość danych, które może zawierać, jest opcjonalna. Mogą one obejmować kody partii i serii, numery seryjne, daty ważności i daty produkcji. Krótko mówiąc, danymi opcjonalnymi mogą być dowolne dane, które producent lub firma nakładająca etykietę uzna za niezbędne do identyfikacji wyrobów.
Każda etykieta UDI musi przedstawiać te informacje w dwóch postaciach:
- postać czytelna dla człowieka (zwykły tekst)
- postać do odczytu maszynowego (przez czytnik kodów kreskowych lub czytnik RFID)
Wszędzie tam, gdzie wyrób może spełniać wiele zastosowań medycznych, identyfikator UDI musi być umieszczony bezpośrednio na wyrobie, a nie na jego opakowaniu. Zasada dotyczy także wyrobów, których można używać wielokrotnie.
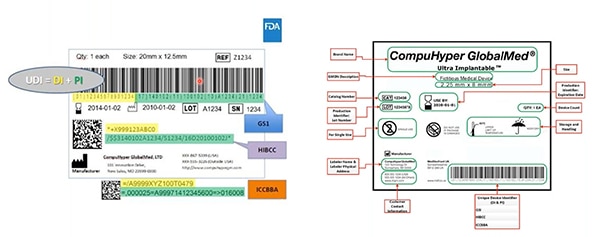 Ilustracja 2: wydające identyfikatory UDI agencje GS1, HIBCC i ICCBBA tworzą kody UDI, przydzielają dopuszczalną symbolikę identyfikatorów UDI, określają technologie mogące współpracować z identyfikatorami UDI oraz określają wymaganą jakość znaków UDI. W tym przykładzie kolorem żółtym oznaczono identyfikator urządzenia, a kolorem zielonym wyróżniono identyfikatory produkcji. Inne elementy obejmują informacje czytelne dla człowieka, które są również zakodowane w kodzie kreskowym do odczytu maszynowego. (Źródło ilustracji: FDA)
Ilustracja 2: wydające identyfikatory UDI agencje GS1, HIBCC i ICCBBA tworzą kody UDI, przydzielają dopuszczalną symbolikę identyfikatorów UDI, określają technologie mogące współpracować z identyfikatorami UDI oraz określają wymaganą jakość znaków UDI. W tym przykładzie kolorem żółtym oznaczono identyfikator urządzenia, a kolorem zielonym wyróżniono identyfikatory produkcji. Inne elementy obejmują informacje czytelne dla człowieka, które są również zakodowane w kodzie kreskowym do odczytu maszynowego. (Źródło ilustracji: FDA)
Wszystkie wyroby muszą być zarejestrowane w globalnej bazie danych UDI, aby umożliwić ich śledzenie w przypadku wycofania z rynku i zapewnić publiczny dostęp do informacji o danym wyrobie. Agencje wydające, akredytowane przez FDA, są upoważnione do tworzenia unikalnych identyfikatorów dla producentów wyrobów w celu umieszczania ich na produktach.
Powiązany raport techniczny: być na bieżąco z identyfikowalnością
Technologie i techniki skanowania identyfikatorów UDI
Etykiety UDI można weryfikować na kilka sposobów na całej drodze od produkcji do użycia.
Weryfikacja w linii produkcyjnej jest wykonywana przez technologie zintegrowane z większymi maszynami w celu szybkiego i dokładnego przetwarzania dużej liczby produktów w trakcie ich produkcji. Technologie te, wspierane przez zaawansowane oprogramowanie, czasami przybierają formę przemysłowych drukarek etykiet. Drukarki te mogą wykonywać własną weryfikację na linii produkcyjnej, aby potwierdzić, że informacje UDI są czytelne zgodnie z rygorystycznymi standardami branżowymi natychmiast po ich utworzeniu w momencie produkcji etykiety. Na przykład weryfikatory Omron Automation V275 są przeznaczone do użytku z drukarkami termicznymi Zebra w celu zapewnienia zgodności z normą ISO 15426 i standardami organu wydającego GS1 w zakresie zgodności z przepisami FDA.
Powiązane tematy: rozwiązania Omron w zakresie identyfikowalności
W innych przypadkach weryfikacja w linii przyjmuje formę wyspecjalizowanego widzenia maszynowego zainstalowanego po bokach przenośników na zautomatyzowanych liniach produkcyjnych. Obejmuje to odczyt kodów kreskowych w celu bardzo szybkiej i dokładnej weryfikacji etykiet UDI na produktach o dużym zróżnicowaniu na szybkich liniach produkcyjnych. Oferta MicroHAWK firmy Omron Automation wyróżnia się w tym obszarze dzięki zaawansowanym czujnikom uzupełnionym zminiaturyzowaną konstrukcją i opcjami łączności, które obejmują Ethernet/IP i PROFINET.
Powiązane tematy: unikanie odpowiedzialności wynikającej z niewłaściwego oznakowania
Natomiast weryfikacja identyfikatorów UDI offline jest najbardziej odpowiednia do zbiorczego pobierania próbek etykiet w celu zapewnienia jakości. Weryfikacja offline, często wykorzystywana do badania próbek, gdy wyroby medyczne opuszczają placówkę lub do niej docierają, może uzupełniać systemy weryfikacji online na wcześniejszych etapach dystrybucji.
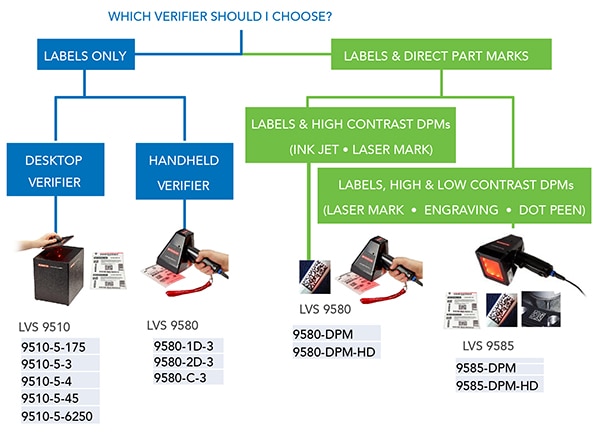 Rysunek 3: identyfikatory UDI umieszczane bezpośrednio na produktach wymagają innych weryfikatorów niż stosowane w przypadku identyfikatorów UDI drukowanych na naklejanych etykietach. (Źródło ilustracji: Omron Automation)
Rysunek 3: identyfikatory UDI umieszczane bezpośrednio na produktach wymagają innych weryfikatorów niż stosowane w przypadku identyfikatorów UDI drukowanych na naklejanych etykietach. (Źródło ilustracji: Omron Automation)
W rzeczywistości wszystkie czynności związane z dystrybucją medyczną i opieką zdrowotną mogą odnieść korzyści ze stosowania weryfikatorów zgodnych z normami ISO. Warto rozważyć produkty firmy Omron z serii LVS 95XX do weryfikacji offline identyfikatorów UDI. Są one stosowane:
- Na stacjach znakowania laserowego i drukarkach etykiet, gdzie tworzone są kody
- W miejscach, gdzie kody są nakładane na produkty, które mogą, ale nie muszą być oddzielone od obszaru tworzenia kodów
- Na stacjach kontroli jakości, gdzie sprawdzane są szablony, formatowanie i inne elementy kodu
Określanie specyfikacji wariantów weryfikatorów UDI w trybie offline
Wybór najbardziej odpowiedniego weryfikatora UDI offline dla danego zastosowania zależy od kilku parametrów.
Rozmiar kodu kreskowego: duże kody kreskowe są często łatwiejsze do zeskanowania dzięki identyfikatorom o dużym polu widzenia, określonym przez ogniskową obiektywu i rozmiar czujnika. Weźmy pod uwagę identyfikatory UDI LVS-9510 firmy Omron Automation. Ta seria produktów może czytać zarówno etykiety liniowe, jak i 2D. Każda z pięciu różnych wersji ma inne pole widzenia, dzięki czemu projektanci mogą wybrać wersję zgodną z rozmiarem kodu kreskowego wymagającego weryfikacji. Funkcja łączenia umożliwia ocenianie kodów kreskowych wykraczających poza pole widzenia.
Ponadto wszystkie modele LVS-9510 mogą automatycznie określać symbolikę i przysłonę potrzebną do oceny kodu oraz identyfikować i wyróżniać problematyczne miejsca.
 Ilustracja 4: weryfikacja kodów kreskowych zgodna z normą ISO jest łatwiejsza dzięki urządzeniom, które mogą weryfikować zarówno kody liniowe (1D), jak i dwuwymiarowe (2D). Niektóre z takich urządzeń określają symbolikę i przesłonę potrzebną do oceny kodów oraz identyfikują i zaznaczają problemy. Pokazane tutaj urządzenie LVS-9510 posiada funkcję łączenia, która umożliwia ocenę kodów kreskowych większych niż pole widzenia. (Źródło ilustracji: Omron Automation)
Ilustracja 4: weryfikacja kodów kreskowych zgodna z normą ISO jest łatwiejsza dzięki urządzeniom, które mogą weryfikować zarówno kody liniowe (1D), jak i dwuwymiarowe (2D). Niektóre z takich urządzeń określają symbolikę i przesłonę potrzebną do oceny kodów oraz identyfikują i zaznaczają problemy. Pokazane tutaj urządzenie LVS-9510 posiada funkcję łączenia, która umożliwia ocenę kodów kreskowych większych niż pole widzenia. (Źródło ilustracji: Omron Automation)
Typ kodu kreskowego: skanery muszą odczytywać formaty kodów kreskowych przydzielone przez organy wydające, znane jako HIBCC, ICCBBA lub (najczęściej od 2023 r.) GS1. GS1 narzuca rozmiar, format i rozdzielczość identyfikatorów UPC, liniowych kodów kreskowych i dwuwymiarowych kodów kreskowych typu data-matrix.
Położenie oznaczenia UDI: weźmy pod uwagę bezpośrednie znakowanie części (DPM) wyrobów medycznych. Oznaczenia te mogą być niezwykle małe, zwłaszcza gdy identyfikują narzędzia chirurgiczne i wszczepiane wyroby medyczne. Aby odczytywać i weryfikować takie identyfikatory UDI nanoszone bezpośrednio na części (DPM), ręczne weryfikatory Omron LVS-9580 i LVS-9585 o ultrawysokiej gęstości są wyposażone w specjalistyczną soczewkę, która może sprawdzać ogromną różnorodność oznaczeń bezpośrednich, w tym nawet o rozmiarach komórki do 0,002 cala. Soczewki klasy przemysłowej wewnątrz urządzeń LVS-9580 i LVS-9585 zapewniają stałą dokładność odczytu. Najbardziej zaawansowane technologie oświetlenia wewnątrz skanerów zapewniają duże możliwości sterowania i kalibracji. Wraz z wieloma polami widzenia, oświetlenie umożliwia natychmiastową optymalizację przechwyconych obrazów UDI. Jest to szczególnie ważne, ponieważ norma dotycząca kodów nie pozwala na żadne późniejsze poprawki ani manipulacje obrazem.
Więcej o oprogramowaniu skanera UDI
Aby zapewnić maksymalną skuteczność, oprogramowanie UDI wspierające sprzęt weryfikatora musi prezentować informacje diagnostyczne w intuicyjnym formacie. Oprogramowanie to musi oceniać kody UDI zgodnie z parametrami zdefiniowanymi przez normę ISO (przede wszystkim, aby potwierdzić ich czytelność) i powinno również śledzić problemy związane z pogarszającą się jakością w serii skanów UDI.
Do każdego z urządzeń skanujących identyfikatory UDI Firma Omron dołącza całe niezbędne oprogramowanie. Oprogramowanie jest regularnie aktualizowane, aby dotrzymać kroku szybko zmieniającym się regulacjom i nowym przepisom branżowym.
Główną funkcją oprogramowania skanera firmy Omron jest obsługa składni kodu. Krótko mówiąc, każdy kod kreskowy lub kod 2D musi umożliwiać dokładne wyodrębnienie wszystkich istotnych informacji, w tym typu produktu, numeru partii, odpowiedniej ilości, daty ważności, informacji o wysyłce itp. Wynikowe ciągi danych muszą być sformatowane w określony sposób, aby dotrzymywać kroku zmieniającym się wymaganiom, metodologiom i przeznaczeniom wyrobów medycznych.
Regularnie aktualizowane oprogramowanie od producenta skanera gwarantuje, że użytkownicy końcowi będą na bieżąco, nawet gdy pojawią się nowe przepisy.
Podsumowanie
Amerykańskie wojsko dążyło kiedyś do pełnego wykorzystania systemu śledzenia produktów UID, podobnego do systemu UDI w branży medycznej. Jego celem było ograniczenie masowego marnotrawstwa związanego z zagubionymi, zduplikowanymi i nierozliczonymi dostawami w instalacjach wojskowych, w tym wszystkiego, od gotowego uzbrojenia Raytheon po płytki sterujące dostarczone przez małą firmę do jakiegoś specjalistycznego zastosowania. Obecnie identyfikatory UID są wykorzystywane w różnym stopniu.
Taki sam los nie spotka obowiązkowych oznaczeń UDI.
Mantra stymulująca wprowadzanie identyfikatorów UDI jest prosta: etykieta jest produktem. W końcu nieprawidłowa etykieta może spowodować łańcuch zdarzeń, który marnuje czas personelu i prowadzi do wyrzucenia wyrobu medycznego. W związku z tym identyfikatory UDI muszą znajdować się na wszystkich warstwach opakowania, takich jak sam wyrób jednostkowy, opakowanie, pakiet, skrzynia i paleta. Identyfikatory UDI na sterylnych urządzeniach medycznych wewnątrz sterylnie zamkniętych opakowań są szczególnie ważne, ponieważ naruszenie opakowania w celu weryfikacji typu wyrobu jest niedopuszczalne.
Ponieważ agencja FDA wymaga pełnego przestrzegania dyrektyw dotyczących unikalnej identyfikacji wyrobów medycznych (UDI) od 24 września 2023 r., zaawansowane technologie skanowania do weryfikacji produktów medycznych staną się bardzo ważne dla producentów automatyki, a także konstruktorów maszyn i użytkowników końcowych, którym służą.
Takie skanery spełniają bardzo szczegółowe wymagania FDA w zakresie identyfikacji UDI dotyczące potwierdzania etykiet na szerokiej gamie sprzętu laboratoryjnego, medycznego i do diagnostyki klinicznej. Weryfikatory kodów kreskowych offline - maksymalizują identyfikowalność, wykorzystanie zintegrowanego widzenia maszynowego i zaawansowane czytniki DPM.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






